Confira seu desempenho na prova EsPCEX! O concurso da Escola Preparatória de Cadetes do Exército – EsPCEx ofertou 440 vagas para o público feminino e masculino.
Você participou das provas nos dias 13 e 14 de setembro? Então acompanhe o gabarito EsPCEX extraoficial, elaborado pelos professores especialistas do Gran.
Preparamos comentários e análises exclusivas sobre as questões nesse conteúdo!
Confira a seguir mais informações sobre a prova EsPCEX.

Navegue pelo e saiba todos os detalhes sobre o Gabarito EsPCEX:
- Gabarito Extraoficial
- Comentários
- Gabarito Preliminar
- Recursos
- Cronograma
- Etapas
- Análise
- Resumo Concurso EsPCEX
| Destaques: |
Gabarito EsPCEX: gabarito extraoficial
Os professores do Gran prepararam o Gabarito EsPCEx Extraoficial, trazendo a correção completa das questões, com comentários técnicos e análises dos nossos professores para auxiliar na correção da sua prova e descobrir o seu desempenho.
Gabarito EsPCEX: comentários
O Gran traz o gabarito extraoficial das questões da prova EsPCEx comentadas por nossos professores especialistas.
Esse conteúdo está sendo atualizado em tempo real conforme o recebimentos dos comentários.
Veja as disciplinas da prova EsPCEx a seguir:
Sábado:
Domingo:
Gabarito EsPCEX: Língua Portuguesa
Questões de 01 a 20 – Prof. Gustavo Silva
Questão 1
GABARITO PRELIMINAR: E
Efetivamente se verifica no trecho assinalado o efeito irônico criado por Machado de Assis, ao unir elementos de naturezas distintas: “perna quebrada”, que diz respeito a algo concreto, físico, e o “desejo de salvar ninguém”, que se refere algo de natureza abstrata e psicológica. Além disso, o uso de “ninguém” em vez de “alguém” reforça o tom irônico do autor e o sentimento de decepção do oficial. Em vista disso, o item E apresenta a interpretação mais completa.
Questão 2
GABARITO PRELIMINAR: B
O trecho “…fez resumidamente a narração que me ficou na memória e aqui vai tal qual.” indica que Machado de Assis está reproduzindo a narração tal como Abel a contou, sem alterações, apenas reproduzindo o que ouvira, sem acrescentar o “pico” e a “alma própria” que o amigo imprimia às suas histórias.
Questão 3
GABARITO PRELIMINAR: E
No texto, Manuel Bandeira relata que ouviu a história diretamente do oficial da marinha inglesa, enquanto ambos estavam internados no Hospital dos Estrangeiros. Posteriormente, ele contou essa história para Abel Ferreira de Matos, que por sua vez conhecia Machado de Assis e transmitiu a este último a narrativa. Logo, a alternativa que indica a correta sequência de transmissão é a do item E.
Questão 4
GABARITO PRELIMINAR: A
O polissíndeto – que consiste no uso reiterado da conjunção coordenativa aditiva “E” –, no contexto, revela a intenção de Manuel Bandeira de sugerir os movimentos contínuos e vigorosos da criatividade machadiana. Cabe observar que não há no texto referência expressa à remissão ao estilo do texto bíblico, mas tão só certo tom de julgamento moral ao se mencionar “iniquidade divina” e “iniquidade humana”, o que mostra que, ao fazer essa associação, o examinador faz uma inferência interpretativa que vai para além dos elementos do texto. Contudo, como o item A é o único que apresenta a ideia do vigor criativo associado ao polissíndeto (que realmente está lá), ela se torna a mais plausível.
Questão 5
GABARITO PRELIMINAR: B
O preposicionamento do objeto direto “Machado” ocorre para evitar ambiguidade em vista do emprego do nome de pessoa também na função de sujeito. Situação similar ocorre no item B.
Questão 6
GABARITO PRELIMINAR: E
A separação silábica do termo destacado se apresentaria desta forma: prin-ci-pi-a. Verifica-se aí um hiato (i-a) na sílababa tônica.
Questão 7
GABARITO PRELIMINAR: C
O discurso direto consiste na reprodução literal da fala do personagem do texto a qual é indicada por travessões ou parênteses. Isso ocorre somente no item III (“É um conto para Machado de Assis”) e IV (“Vocês, materialistas…” e “Eu, ma…materialista? Absolutamente!”).
Questão 8
GABARITO PRELIMINAR: A
Como há referência a pessoa e a anteposição de preposição, o relativo “que” em “de que falei” pode corretamente ser substituído pelo relativo quem: “de quem falei”. Todas as outras alternativas apresentam erro gramatical ou alteração semântica.
Questão 9
GABARITO PRELIMINAR: A
Espiritista >> espírito + -ista (sufixo) >> sufixação.
Desnorteado >> des- (prefixo) + norte + -ado (sufixo) >> parassíntese
Infeliz >> in- (prefixo) + feliz >> prefixação.
Questão 10
GABARITO PRELIMINAR: C
Tanto o trecho “em que parece” (= no qual parece) quanto “que era um crente” (= o qual era um crente) ostentam pronomes relativos antecedidos de pontuação. Isso implica afirmar que se trata de duas orações subordinadas adjetivas explicativas.
Questão 11
GABARITO PRELIMINAR: B
Trata-se de questão que pode gerar polêmica; contudo, a resposta mais adequada é a alternativa B. Em A, não ocorre crase em vista de haver palavra masculina; em C, não ocorre crase porque a cidade o nome Montevidéu, no contexto, não é antecedida de artigo, mas outros nomes de cidades que aceitam o artigo feminino antes de si aceitariam crase; no item D, não ocorre crase porque se trata de substantivo feminino no plural empregado em sentido indefinido; no item E, não se trata da presença ou ausência de adjetivo, pois, em outro contexto, o adjetivo poderia proporcionar a presença da crase.
Questão 12
GABARITO PRELIMINAR: B
O advérbio “absolutamente” pode ser usado para afirmações ou negações. No contexto, Machado de Assis queria negar que era materialista, sendo assim, o sentido que se encaixa ali é “de modo algum”.
Questão 13
GABARITO PRELIMINAR: D
O trecho em questão pode ser assim entendido: Não inventei aquilo o qual vou contar, nem o inventou o meu amigo Abel. Nesse contexto, verifica-se a presença de oração subordinada adjetiva restritiva (o qual vou contar) e de oração coordenada aditiva (nem o inventou o meu amigo Abel). Disso decorre a correção do item D como gabarito.
Questão 14
GABARITO PRELIMINAR: D
No trecho assinalado, o termo “morre não morre” é uma expressão popular que se refere ao estado do sujeito “eu” durante o internamento e indica uma condição ou estado em que se encontrava. Por atribuir uma característica ou estado ao sujeito, tal expressão funciona como predicativo do sujeito.
Questão 15
GABARITO PRELIMINAR: B
No contexto, tem-se construção na qual não se identifica prontamente o agente do processo verbal e o verbo transitivo direto (ver). Tal construção indica que o pronome “se” atua como pronome apassivador: parecia ser vista a figura de uma mulher.
Questão 16
GABARITO PRELIMINAR: D
O pronome “o” repete o objeto direto anterior: Abel ouviu o caso do conto “O incêndio” de mim. Logo, tem-se objeto direto pleonástico.
Questão 17
GABARITO PRELIMINAR: C
Manuel Bandeira foi, de fato, um dos nomes centrais da primeira fase do Modernismo brasileiro, ao lado de Mário de Andrade e Oswald de Andrade. Bandeira se destacou por sua poesia lírica, intimista e profundamente humana, com forte influência do Simbolismo e do Modernismo, mas sem a postura radical de ruptura total com o passado que caracterizava outros modernistas.
Questão 18
GABARITO PRELIMINAR: C
O autor descrito no trecho é Cruz e Sousa, principal representante do Simbolismo no Brasil. Sua poesia é marcada por profunda angústia metafísica, investigação filosófica e espiritual, desejo de transcendência e fuga da realidade material e estética simbolista com musicalidade, subjetividade e misticismo. Além disso, o texto menciona o drama racial e pessoal, o que se refere diretamente à condição de Cruz e Sousa como poeta negro em uma sociedade marcada pelo racismo estrutural — elemento que influenciou fortemente sua obra e sua visão de mundo.
Questão 19
GABARITO PRELIMINAR: B
No poema, Manuel Bandeira celebra a linguagem popular e cotidiana, valorizando o modo como o povo fala – mesmo que seja considerado “errado” pela norma culta. Ele afirma: “Vinha da boca do povo na língua errada do povo / Língua certa do povo / Porque ele é que fala gostoso o português do Brasil”. Esse trecho é um manifesto poético em defesa da oralidade brasileira como expressão legítima da língua, alinhando-se diretamente à proposta da primeira geração modernista, que buscava romper com o formalismo acadêmico e aproximar a literatura da realidade nacional.
Questão 20
GABARITO PRELIMINAR: E
O comentário de Abel — “É um conto para Machado de Assis” — surge após ele ouvir uma história marcada por injustiça e sofrimento, que o deixa desnorteado e infeliz, apesar de sua fé. Ao associar esse tipo de narrativa a Machado de Assis, Abel está reconhecendo uma característica marcante do autor: seu olhar pessimista e desencantado sobre a condição humana e sobre as instituições divinas e sociais.
Gabarito EsPCEX: Física
Questões de 21 a 32 – Prof. Hérico Avohai
QUESTÃO NÚMERO: 21
GABARITO PRELIMINAR: C
COMENTÁRIO:
Se a força resultante é não nula, pela dinâmica newtoniana temos 𝑎 = 𝐹res/𝑚 ≠ 0;
Logo, a velocidade do ponto material varia (em módulo e/ou direção). As outras opções falham: [A] e [D] confundem ausência de resultante com “não há forças” (pode haver forças que se anulam); [B] é falsa porque “módulo da velocidade constante” não garante 𝑎 = 0 — há o caso de movimento circular uniforme, com 𝑣 v constante e aceleração centrípeta diferente de zero; [E] é absurda (inércia não se perde). Assim, a única afirmação sempre verdadeira é a [C].
QUESTÃO NÚMERO: 22
GABARITO PRELIMINAR: A
COMENTÁRIO:
Como o pneu gira rigidamente a 500 rpm, todos os pontos têm o mesmo período 𝑇, a mesma frequência 𝑓 e a mesma velocidade angular 𝜔; o que muda com o raio 𝑟 é a velocidade linear 𝑣 =𝜔𝑟 e, sobretudo, a aceleração centrípeta 𝑎𝑐 = 𝜔2𝑟, que cresce linearmente com r. Portanto, mais perto do centro (menor r) a aceleração centrípeta é menor, enquanto as alternativas que falam em variação de 𝑇, 𝑓 ou 𝜔 com a posição estão incorretas.
QUESTÃO NÚMERO: 23
GABARITO PRELIMINAR: C
COMENTÁRIO:
Tomando torques em torno do apoio 𝑂: a força magnética na haste vale 𝐹𝑚 = 𝐵𝐼𝐿 = 𝐵𝐼(10𝑑) e atua para baixo no centro geométrico de 𝑃𝑄, a 3𝑑 de 𝑂. Para que a haste permaneça horizontal, o torque magnético (sentido horário) deve ser compensado por um aumento da força da mola na posição 𝐻 (sentido anti-horário), a 𝑂𝐻=1,6𝑑. Logo,
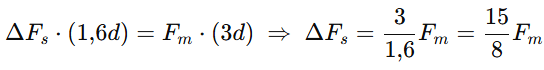
A mola puxa a haste para cima e o cilindro para baixo; assim, o empuxo exigido aumenta de Δ𝐹𝑠, fazendo o nível submergir e a parte emersa variar de
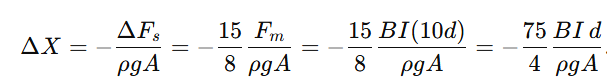
QUESTÃO NÚMERO: 24
GABARITO PRELIMINAR: B
COMENTÁRIO:
a) “cargas puntiformes deslocam-se espontaneamente para regiões de menor potencial elétrico.”
Isso só vale para cargas positivas; as negativas vão espontaneamente para regiões de maior potencial. Como o enunciado fala genericamente em “cargas elétricas”, está incorreta.
b) “em campo elétrico uniforme, as cargas puntiformes ficam sujeitas a uma força elétrica constante.”
Correto: no campo uniforme, 𝐸 é constante → 𝐹 = 𝑞𝐸 também é constante.
c) “cargas positivas aumentam sua energia potencial ao se deslocarem sobre uma mesma superfície equipotencial.”
Errada. Em uma superfície equipotencial, 𝑉 é constante → Δ𝑈 = 𝑞Δ𝑉 = 0. Não há aumento de energia potencial.
d) “cargas negativas aumentam sua energia potencial ao se deslocarem espontaneamente em campo uniforme.”
Errada. O movimento espontâneo sempre diminui a energia potencial elétrica (seja carga positiva ou negativa).
e) “superfície equipotencial é uma superfície cujos pontos têm o mesmo vetor campo elétrico.”
Errada: equipotencial significa mesmo potencial elétrico escalar, não o mesmo vetor de campo.
QUESTÃO NÚMERO: 25
GABARITO PRELIMINAR: A
COMENTÁRIO:
Em regime estacionário (corrente contínua), capacitor é circuito aberto, então não circula corrente pelos resistores e, portanto, não há queda de tensão em nenhum 𝑅: todos os pontos ligados ao mesmo barramento por resistores ficam equipotenciais. Observando o desenho, C1 e C2 estão entre o barramento superior e o barramento central; a diferença de potencial entre esses dois barramentos é fixada apenas pela fonte ideal 𝐸1 (os resistores verticais não caem tensão), logo 𝑉C1 = 𝑉C2 = 𝐸1 e 𝑄C1 = 𝑄C2 = 𝐶𝐸1. Já C3 tem seus dois terminais ligados ao mesmo potencial do barramento central (os caminhos até o barramento inferior passam por resistores sem corrente, de modo que os dois lados de C3 ficam no mesmo potencial), resultando em 𝑉C3 = 0 e 𝑄C3 = 0. Portanto, as cargas são (𝐶𝐸1, 𝐶𝐸1, 0).
QUESTÃO NÚMERO: 26
GABARITO PRELIMINAR: B
COMENTÁRIO:
A entropia está ligada à 2ª Lei da Termodinâmica, que afirma que em processos naturais a entropia total do universo aumenta ou, no melhor caso, permanece constante (em processos reversíveis).
- a) Errada. Diz que a entropia permanece constante só em processos reversíveis ideais, não no universo real.
- b) Certa. “À medida que o universo evolui, diminui a possibilidade de obter trabalho de um sistema”: conforme a entropia aumenta, a energia útil disponível para trabalho diminui.
- c) Errada. “Tendem para um estado mais ordenado” é o contrário, os fenômenos naturais evoluem para estados mais desordenados.
- d) Errada. “Transformações irreversíveis diminuem a entropia”. Elas aumentam a entropia do universo.
- e) Errada. “É possível transformar integralmente trabalho em calor em um ciclo” isso está invertido; trabalho pode se transformar integralmente em calor, mas o enunciado fala de ciclo termodinâmico (onde não há conversão integral inversa).
QUESTÃO NÚMERO: 27
GABARITO PRELIMINAR: D
COMENTÁRIO:

QUESTÃO NÚMERO: 28
GABARITO PRELIMINAR: C
COMENTÁRIO:
O rendimento de Carnot é:

QUESTÃO NÚMERO: 29
GABARITO PRELIMINAR: C
COMENTÁRIO:
Calor necessário:

QUESTÃO NÚMERO: 30
GABARITO PRELIMINAR: E
COMENTÁRIO:
Imagem “imprópria” = imagem no infinito, o que ocorre quando a distância objeto–espelho vale a distância focal d = 𝑓 = 10 cm. No instante 𝑡 = 0 a separação é 𝑑0 = 8 cm. Se tomarmos o eixo para a direita, o espelho move-se com 𝑣𝑒 = + 3 cm/s e o objeto com módulo 𝑣𝑝 = 1 cm/s (sentido não especificado). A distância relativa é
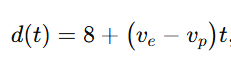
com 𝑣𝑒 = 3 cm/s. Se o objeto vai para a direita (𝑣𝑝=+1):
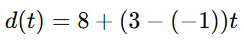
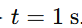
QUESTÃO NÚMERO: 31
GABARITO PRELIMINAR: B
COMENTÁRIO:
Como as velocidades se somam vetorialmente (referenciais galileanos), a velocidade inicial da flecha em relação ao solo é a soma da velocidade do arqueiro com a velocidade da flecha em relação ao arqueiro. Componentes da flecha “vista” pelo arqueiro (18 m/s a 45°), como o ângulo é 45º, vx,rel = vy.rel:

QUESTÃO NÚMERO: 32
GABARITO PRELIMINAR: E
COMENTÁRIO:
Massa total:

Gabarito EsPCEX: Química
Questões de 33 a 44 – Prof. Marina Baccarin
Questão 33
GABARITO PRELIMINAR: LETRA A.
COMENTÁRIO: Vamos aos cálculos:
Passo 1: Calcular a massa máxima de arsênio
O limite é de 0,15 mg de arsênio por kg de alimento. Primeiro, convertemos a massa do alimento de gramas para quilogramas:
250 g = 0,250 kg
Agora, usamos uma regra de três para encontrar a massa máxima de arsênio na amostra:
0,15 mg de As ———- 1 kg de alimento
x mg de As ————— 0,250 kg de alimento
x = 0,15 . 0,250
x = 0,0375 mg de Arsênio
Passo 2: Calcular a quantidade de átomos
Olhando na tabela tem-se que a massa atômica do As é 75 u. Transformando em massa molar tem-se que é 75g/mol. Vamos então montar uma regra de três simples:
75000 mg —– 6 . 1023
0,0375 mg—- Y
Y = (0,0375 . 6 . 1023)/75000
Y = 3 . 1017 átomos de As
Questão 34
GABARITO PRELIMINAR: LETRA E.
COMENTÁRIO:
Olhando na tabela periódica temos que Bi se encontra no período 6, logo sua camada de valência é a camada 6. (Já elimina as letras b e d).
A distribuição eletrônica dos 83 elétrons do Bi, segundo o diagrama de energia, é:
1s² 2s² 2p⁶ 3s² 3p⁶ 4s² 3d¹⁰ 4p⁶ 5s² 4d¹⁰ 5p⁶ 6s² 4f¹⁴ 5d¹⁰ 6p³
Subnível mais energético: É o último subnível da distribuição eletrônica. Portanto, o subnível mais energético é o 6p³.
Camada de valência: É a camada mais externa do átomo, ou seja, aquela com o maior número quântico principal (o número na frente da letra do subnível). Neste caso, a camada mais externa é a 6ª camada. Ela é composta pelos subníveis 6s² e 6p³.
Questão 35
GABARITO PRELIMINAR: LETRA D.
COMENTÁRIO: Vamos analisar cada afirmativa:
I) Incorreta. Os 6 carbonos do anel aromático possuem, sim, hibridização sp². No entanto, o carbono do grupo carbonila (C=O) na cadeia lateral também tem hibridização sp². Portanto, a molécula possui um total de 7 carbonos sp², e não 6. A hibridização sp2 é quando o carbono faz uma ligação simples e duas duplas.
II) Correta. Na molécula abaixo, os átomos de carbono foram destacados de vermelho e os átomos de hidrogênio de verde.
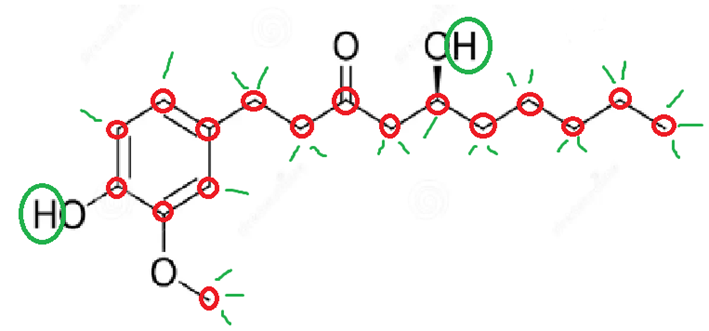
III) Correta. A molécula possui um anel benzênico, que é um grupo aromático.
IV) Correta. A função éter é o átomo de oxigênio entre os carbonos.
V) Incorreta. Vamos analisar os termos:
Cadeia mista: Correto, pois possui uma parte cíclica (o anel) e uma parte acíclica (a cadeia lateral).
Homogênea: Incorreto. A cadeia é heterogênea porque apresenta átomos de oxigênio (heteroátomos) entre os carbonos (no grupo éter).
Saturada: Incorreto. A cadeia é insaturada devido às duplas ligações presentes no anel aromático.
Questão 36
GABARITO PRELIMINAR: LETRA B.
COMENTÁRIO: A reação de dinitração do benzeno forma majoritariamente o 1,3-dinitrobenzeno (ou meta-dinitrobenzeno).
Vamos entender o porquê:
Primeira Nitração: A primeira etapa é a nitração do benzeno, que forma o nitrobenzeno.
Benzeno + HNO₃ (na presença de H₂SO₄) → Nitrobenzeno
O grupo nitro (-NO₂) que foi adicionado ao anel é um grupo desativante e orientador meta. Isso quer dizer que ele retira densidade eletrônica do anel aromático, tornando-o menos reativo a uma segunda substituição do que o benzeno original.
Por retirar elétrons principalmente das posições orto e para, ele deixa a posição meta como a mais “rica” em elétrons (ou menos “pobre”) e, portanto, o local mais provável para o ataque do segundo eletrófilo (o íon nitrônio, NO₂⁺).
Assim, quando o nitrobenzeno sofre uma nova nitração, o segundo grupo nitro entra na posição meta (posição 3) em relação ao primeiro.
Questão 37
GABARITO PRELIMINAR: LETRA D.
COMENTÁRIO: Vamos analisar cada alternativa:
a) Incorreta. A primeira parte está certa (desloca no sentido de formação de H⁺ e HCO₃⁻), mas a consequência está errada. A formação de H⁺ aumenta a acidez do sangue, não a diminui.
b) Incorreta. O equilíbrio da reação é, de fato, alterado (deslocado para a direita) pelo aumento de CO₂.
c) Incorreta. A constante de equilíbrio (K) de qualquer reação é alterada pela variação de temperatura.
d) Correta. A acidose (aumento da acidez) é o aumento de [H⁺], e isso é causado pelo deslocamento do equilíbrio para a direita devido ao excesso de CO₂.
e) Incorreta. Provoca um aumento na concentração de H⁺, não uma diminuição.
Questão 38
GABARITO PRELIMINAR: LETRA C.
COMENTÁRIO: Vamos analisar cada uma das afirmativas:
I) Incorreta. O polietileno é formado pela quebra da ligação dupla da molécula de eteno (CH₂=CH₂) e a união sucessiva de vários desses monômeros. Esse tipo de reação é chamado de polimerização de adição, não de condensação. Na polimerização de condensação, haveria a eliminação de uma molécula pequena (como a água), o que não acontece aqui.
II) Correta. A estrutura do polietileno consiste em uma longa cadeia formada apenas por átomos de carbono e hidrogênio (-CH₂-CH₂-)n. Compostos formados exclusivamente por carbono e hidrogênio são, por definição, hidrocarbonetos.
III) Incorreta. As ligações de hidrogênio são interações fortes que ocorrem quando o hidrogênio está ligado a átomos muito eletronegativos, como Flúor (F), Oxigênio (O) ou Nitrogênio (N). O polietileno, sendo um hidrocarboneto, não possui esses átomos. Suas interações intermoleculares são do tipo forças de van der Waals (ou dipolo induzido), que são muito mais fracas.
IV) Correta. Como a molécula é formada apenas por carbono e hidrogênio, a diferença de eletronegatividade entre eles é muito baixa, e a geometria da longa cadeia é simétrica. Isso resulta em uma molécula com distribuição de carga elétrica uniforme, caracterizando-a como apolar.
V) Correta. Conforme explicado no item I, a reação de formação do polietileno é uma polimerização de adição, onde monômeros de eteno são “adicionados” uns aos outros.
Questão 39
GABARITO PRELIMINAR: LETRA C.
COMENTÁRIO: Primeiro vamos balancear a equação, isto é, igualar as quantidades de átomos dos dois lados da equação:
2C₂H₂ + 5O₂ → 4CO₂ + 2H₂O
O cálculo da entalpia de uma reação (ΔH°reação) é feito pela diferença entre a soma das entalpias de formação dos produtos e a soma das entalpias de formação dos reagentes, considerando seus coeficientes estequiométricos.
A fórmula é:
ΔH°reação = Σ (ΔH°f produtos) – Σ (ΔH°f reagentes)
Temos então:
ΔH°reação = (4 mol × (-393 kJ/mol) + 2 mol × (-286 kJ/mol)) – (2 mol × (+227 kJ/mol) + 5 mol × (0 kJ/mol))
ΔH°reação = (-1572 -572) – (454)
ΔH°reação = -2600 kJ
O valor de -2600 kJ corresponde à queima de 2 mols de acetileno (C₂H₂), conforme a equação balanceada. A pergunta pede o calor de combustão em kJ/mol, ou seja, para a queima de apenas 1 mol.
Calor de combustão = (-2600 kJ) / 2 mol
Calor de combustão = -1300 kJ/mol
Questão 40
GABARITO PRELIMINAR: LETRA A
COMENTÁRIO: Primeiro vamos balancear a equação, isto é, igualar as quantidades de átomos dos dois lados da equação:
2NH₄NO₃ → 2N₂ + O₂ + 4H₂O
Vamos agora calcular os mols de NH₄NO₃
Primeiro, precisamos da massa molar do nitrato de amônio (NH₄NO₃):
Olhando na tabela periódica, tem-se as seguintes massas molares:
N: 14 g/mol
H: 1 g/mol
O: 16 g/mol
Massa Molar = (2 × 14) + (4 × 1) + (3 × 16) = 28 + 4 + 48 = 80 g/mol
E convertendo a massa dada para gramas, calculamos o número de mols:
Massa = 1,6 kg = 1600 g
Número de mols = massa / massa molar
Número de mols de NH₄NO₃ = 1600 g / 80 g/mol = 20 mols de NH₄NO₃
Vamos então calcular o total de mols de gases produzidos
A proporção estequiométrica é:
2 mols de NH₄NO₃ produzem um total de 2 + 1 + 4 = 7 mols de gases.
Agora, usamos uma regra de três para encontrar os mols de gás produzidos a partir dos 20 mols de reagente que calculamos:
2 mols de NH₄NO₃ ———- 7 mols de gases
20 mols de NH₄NO₃ ——— x
x = (20 × 7) / 2
x = 70 mols de gases totais
Por fim, calculamos o volume usando a Lei dos Gases Ideais. Não se esqueça que a temperatura tem que estar em Kelvin (T(K) = 127 + 273 = 400 K)
PV = nRT
V = (nRT) / P
V = (70 × 0,082 × 400) / 1
V = 70 × 32,8
V = 2296 L
Questão 41
GABARITO PRELIMINAR: LETRA B.
COMENTÁRIO: Temos os seguintes conceitos:
- Meio Hipotônico (Hipo = Menos)
É a solução que possui a menor concentração de soluto em comparação com a outra.
- Meio Hipertônico (Hiper = Mais)
É a solução que possui a maior concentração de soluto em comparação com a outra.
- Meio Isotônico (Iso = Igual)
Ocorre quando as duas soluções têm concentrações de soluto exatamente iguais.
Agora vamos analisar as alternativas:
I) Incorreta. É hipotônico, pois tem baixa concentração do soluto.
II) Correta. Pois tem a mesma concentração.
III) Incorreta. É hipertônico, pois tem alta concentração do soluto.
Questão 42
GABARITO PRELIMINAR: LETRA E.
COMENTÁRIO: Vamos analisar cada uma das afirmativas:
I) Reação química: Al₂(SO₄)₃ + NaOH → Na₂SO₄ + Al(OH)₃
Balanceamento:
Começamos com o Alumínio (Al): temos 2 no reagente, então precisamos de 2 no produto: Al₂(SO₄)₃ + NaOH → Na₂SO₄ + 2Al(OH)₃
Agora, o enxofre (S): temos 3 nos reagentes, então precisamos de 3 nos produtos: Al₂(SO₄)₃ + NaOH → 3Na₂SO₄ + 2Al(OH)₃
Agora o Sódio (Na): temos 3 * 2 = 6 nos produtos, então precisamos de 6 nos reagentes: Al₂(SO₄)₃ + 6NaOH → 3Na₂SO₄ + 2Al(OH)₃
E com estes coeficientes os átomos de oxigênio e hidrogênio já ficam balanceados.
Soma dos coeficientes: 1 + 6 + 3 + 2 = 12
Logo, item correto.
II) Incorreta. No processo de decantação, as partículas mais densas que o líquido tendem a se depositar no fundo do recipiente devido à ação da gravidade. As partículas menos densas flutuariam.
III) Incorreta. Nesta reação dois compostos reagem trocando seus íons entre si (o Al³⁺ troca de lugar com o Na⁺). Esse tipo de reação é classificado como dupla troca ou metátese. Uma reação de simples troca (ou deslocamento) ocorre quando uma substância simples reage com uma composta, deslocando um de seus elementos.
IV) Correta. A filtração é um método de separação de misturas heterogêneas, especificamente entre um sólido insolúvel e um líquido (ou gás). O líquido passa pelo filtro, enquanto o sólido fica retido.
Questão 43
GABARITO PRELIMINAR: LETRA C.
COMENTÁRIO: Vamos analisar cada item:
I) Correta.
II) Incorreta. A definição está trocada. Segundo Lewis, a base é a espécie que doa um par de elétrons, e o ácido é a espécie que recebe.
III) Correta.
IV) Incorreta. As aminas (derivadas da amônia, NH₃) possuem um par de elétrons livre no átomo de nitrogênio. Por isso, elas têm a tendência de receber um próton (H+), atuando como bases de Brønsted-Lowry, e de doar esse par de elétrons, atuando como bases de Lewis. Portanto, as aminas têm caráter básico.
V) Correta. Uma substância pode atuar como ácido em uma reação (doando um próton) e como base em outra (recebendo um próton). A água é o exemplo mais clássico desse comportamento, conhecido como anfoterismo.
Questão 44
GABARITO PRELIMINAR: LETRA E.
COMENTÁRIO: Vamos analisar cada item:
I) Correta. Os íons Cl– perdem elétrons para se transformar no gás Cloro. Portanto, trata-se de uma reação de oxidação (veja que o Nox da espécie química aumenta de -1 para 0). A reação de oxidação ocorre no ânodo.
II) Incorreta. Processo espontâneo ocorre em pilhas e baterias. Na eletrólise o processo é não espontâneo.
III) Incorreta. Pois a água não sofre variação em seu Nox (tanto o H quanto o Oxigênio continuam com carga + 1 e -2, respectivamente). O próprio gás cloro é que atua como agente oxidante e redutor.
IV) Correta. O aumento da concentração dos reagentes desloca o equilíbrio químico a favor da formação dos produtos.
Gabarito EsPCEX: gabarito preliminar
A divulgação dos gabaritos preliminares das provas objetivas estarão disponíveis em 16 de setembro de 2025 a partir das 18h.
Gabarito EsPCEX: recursos
A Interposição de pedidos de revisão dos gabaritos das provas objetivas pode ser feitas até 19 setembro de 2025.
Gabarito EsPCEX: cronograma
- Até 24 de out 25: Divulgação das notas das provas objetivas, da nota mediana de cada uma das provas objetivas e da listagem, em ordem alfabética, dos candidatos aptos à correção da Redação.
- Até 7 de nov 25: Divulgação das notas e dos espelhos das redações corrigidas.
Gabarito EsPCEX: próximas etapas
- 04 de dez 25: Convocação dos aprovados e classificados, para a realização da 2ª etapa do Concurso de Admissão;
- 20 de jan 26: Apresentação dos candidatos classificados convocados para a 2ª etapa do Concurso de Admissão (realização de Inspeção de Saúde, Exame de Aptidão Física, Avaliação Psicológica, Heteroidentificação Complementar e comprovação documental) das 08h às 14h.
Prova EsPCEX: análise
Fez a prova EsPCEX neste final de semana, dia 13 e 14 de setembro? Deixe nos comentários a sua análise sobre a prova.
• O que você achou do nível de dificuldade da prova?
• O conteúdo cobrado na prova estava de acordo com o previsto no edital?
• A banca trouxe alguma inovação na cobrança do conteúdo?
• Havia muitos candidatos ausentes na sua sala?
Saiba mais sobre o Concurso ESPCEX
Prepare-se com o Gran: Assinatura Ilimitada 11
Assine agora e receba acesso IMEDIATO a plataforma que mais aprova em concursos públicos e, o melhor, com acesso às 5 novidades da plataforma: Cronograma com 1 clique, Raio-X, Jornada do Aprovado, Legislação Comentada e a Revisão Inteligente. Faça o teste por 7 dias. O Gran está comprometido com a sua preparação! Satisfação garantida ou seu dinheiro de volta!
*Os cursos para OAB, CFC e Residências não estão disponíveis na Assinatura Ilimitada.
Resumo do Concurso ESPCEX
| Concurso ESPCEX | Escola Preparatória de Cadetes do Exército. |
|---|---|
| Situação Atual | Edital Publicado |
| Banca organizadora | Comissão própria |
| Cargos | Cadete |
| Escolaridade | Nível médio |
| Carreiras | Militar |
| Lotação | Campinas–SP |
| Número de vagas | 440 vagas |
| Remuneração | de R$ 1.339,00 (1° ano do Curso de Formação EsPCEx) |
| Inscrições | 23/03 A 09/05/2025 |
| Taxa de inscrição | de R$ 100 |
| Data da prova objetiva | em 13 e 14/09/2025 |
| Clique aqui para ver o edital ESPCEX | |
Quer ficar por dentro dos concursos públicos abertos e previstos pelo Brasil? Clique nos links abaixo:
Receba gratuitamente no seu celular as principais notícias do mundo dos concursos. Clique no link abaixo e inscreva-se:
![[Preparatórios] Concursos Militares – Cabeçalho](https://blog-static.infra.grancursosonline.com.br/wp-content/uploads/2026/01/15171318/assinatura-de-verdade-concursos-militares-30off-cabecalho.webp)

![[Preparatórios] Concursos Militares – Post](https://blog-static.infra.grancursosonline.com.br/wp-content/uploads/2026/01/15171359/assinatura-de-verdade-concursos-militares-30off-post.webp)